
Logran avance clave contra una grave enfermedad genética
Especialistas del CONICET y de la UBA consiguieron, en estudios in vitro, estabilizar proteínas defectuosas asociadas a la ataxia de Friedreich, un trastorno degenerativo que aún no tiene cura. El trabajo, que forma parte de una línea de investigación que cuenta con un subsidio internacional, abre nuevas posibilidades terapéuticas.
Existen tratamientos que reducen su progresión, pero por ahora no existe cura para la ataxia de Friedreich (AF), una enfermedad genética que afecta aproximadamente a una de cada 50 mil personas y que se caracteriza por el daño progresivo del sistema nervioso y de complicaciones cardiológicas.
En este contexto, científicos del CONICET y de la UBA lograron desarrollar por primera vez nanoanticuerpos específicos que al interior de células fueron capaces de unirse a la proteína blanco cuya deficiencia genera ese trastorno degenerativo. El avance, descrito en la revista Communications Biology, sienta bases para explorar el desarrollo de una estrategia terapéutica innovadora para esa patología.

Asimismo, el laboratorio del investigador del CONICET Javier Santos, uno de los líderes del avance, recibió un subsidio internacional de la Alianza para la Investigación de la Ataxia de Friedreich (FARA, según sus siglas en inglés) para seguir avanzando con esta línea de trabajo.
“La causa molecular de la ataxia de Friedreich (AF), es la disminución de la expresión (producción) de proteína frataxina o la expresión de variantes con función o estabilidad alterada. En este nuevo trabajo logramos estabilizar estas proteínas patológicas en estudios in vitro (de forma aislada) y al interior de células humanas. Actualmente, estamos trabajando con células donadas de forma consentida por pacientes a través de biobancos hospitalarios”, afirma Santos, colíder del avance e investigador del Instituto de Biociencias, Biotecnología y Biología Traslacional (iB3-FBMC) que depende de la Facultad de Ciencias Exactas y Naturales de la UBA. Y continúa: “El avance nos alienta a profundizar esta línea de investigación con la esperanza de contribuir al desarrollo de estrategias terapéuticas superadoras, eficaces, y accesibles para las personas”.
Nanoanticuerpos generados en camélidos
La principal característica de la ataxia de Friedreich es una alteración en los genes que limita la fabricación o resulta en la producción de formas funcionalmente defectuosas de frataxina que está en las mitocondrias (fábricas de metabolitos y cofactores y usinas de energía de las células).
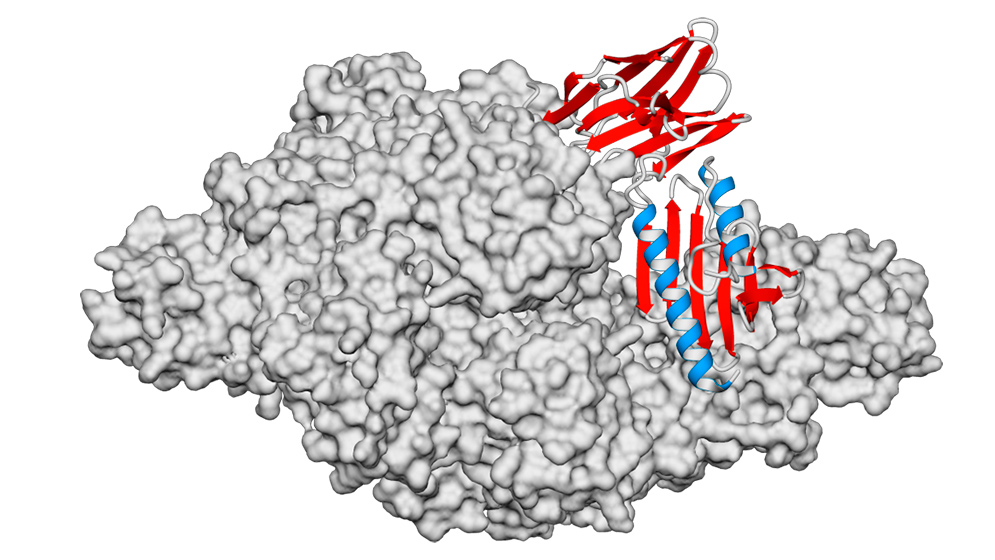
El primer paso en este trabajo fue inmunizar una llama. Se le inyectó la variante silvestre de frataxina de origen humano para que su sistema inmune generase anticuerpos de cadena pesada (dominios VHH) con capacidad de unirse específicamente a las conformaciones correctamente plegadas. La inmunización fue realizada en INTA Castelar con la colaboración de las científicas del CONICET Viviana Parreño y Marina Bok.
Además, el grupo de investigación está desarrollando con apoyo internacional unas variantes muy especiales de estos nanoanticuerpos.
“Los nanoanticuerpos que utilizaremos en la continuación de este trabajo son pequeñas moléculas derivadas de los anticuerpos fabricados por el sistema inmune de los camélidos. Tienen la capacidad de penetrar membranas celulares, ubicarse en mitocondrias y estabilizar proteínas defectuosas de frataxina”, explica María Florencia Pignataro, primera autora del trabajo e investigadora del CONICET en el iB3. Y continúa: “Los nanoanticuerpos constituyen una herramienta útil y versátil para interaccionar con proteínas dentro de la célula por su pequeño tamaño y alta afinidad”.
En esa línea, Santos afirma: “Otro aspecto interesante de nuestra investigación es que observamos que la expresión de los nanoanticuerpos y su localización mitocondrial no afecta ciertas variables celulares como viabilidad, respiración celular y otras funciones. Esta información es alentadora si pensamos en posibles terapias basadas en nanoanticuerpos”.
Para Itatí Ibañez, colíder del trabajo e investigadora del CONICET en el Instituto de Química Física de los Materiales, Medio Ambiente y Energía (INQUIMAE, CONICET-UBA), “el reducido tamaño de los nanoanticuerpos permite que un único vector de terapia génica pueda transportar varios de ellos o incorporar formatos multivalentes, lo que representa una ventaja significativa frente a otras moléculas terapéuticas”.
Además, afirma la investigadora, “los nanoanticuerpos pueden modificarse con gran facilidad para favorecer su penetración en tejidos y células, ampliando así su potencial y facilitando su aplicación como agentes terapéuticos. Se trata de una herramienta altamente versátil, con un creciente interés tanto en biotecnología como en aplicaciones clínicas y con mucho potencial para poder ser desarrolladas como especialidades medicinales para la ataxia de Friedreich”.
Los conocimientos obtenidos en este trabajo “podrían ayudar a identificar nuevas estrategias terapéuticas para restaurar la función mitocondrial en los tejidos afectados por la ataxia de Friedreich”, destaca Santos. Y concluye: “Continuaremos con más investigaciones con el objetivo de probar esta estrategia en modelos preclínicos, un paso previo y crucial para evaluar su seguridad y eficacia en ensayos clínicos”.
Para la obtención de células de pacientes, el equipo de investigación mantiene una colaboración con el Hospital Italiano de Buenos Aires, con los doctores Diego Santoro, Marcelo Ielpi y Leandro D. Burgos Pratx, coordinador del Biobanco. Asimismo, trabajaron en cooperación con el laboratorio de Juan Antonio Hermoso en el Instituto de Química-Física “Blas Cabrera”, en Madrid, España.
También participaron del trabajo, Antonella Vila, Hernán G. Gentili, Natalia Brenda Fernández, Alba Garay-Alvarez, Naira Antonia Rodríguez, Augusto E. García y Julián Grossi, del iB3 y del Departamento de Fisiología, Biología Molecular y Celular (DFBMC, FCEN-UBA); María Florencia Pavan, del INQUIMAE; Martín Noguera, del Instituto de Química y Fisicoquímica Biológicas “Prof. Alejandro C. Paladini” (IQUIFIB, CONICET-UBA); Martín Aran, del CONICET y de la Fundación Instituto Leloir; Rafael Molina, del Instituto de Química-Física “Blas Cabrera”; e Inés G. Muñoz, del Centro Nacional de Investigaciones Oncológicas (CNIO), en Madrid, España.
Archivos
- abril 2026
- marzo 2026
- febrero 2026
- enero 2026
- diciembre 2025
- noviembre 2025
- octubre 2025
- septiembre 2025
- agosto 2025
- julio 2025
- junio 2025
- mayo 2025
- abril 2025
- marzo 2025
- febrero 2025
- enero 2025
- diciembre 2024
- noviembre 2024
- octubre 2024
- septiembre 2024
- agosto 2024
- julio 2024
- junio 2024
- mayo 2024
- abril 2024
- marzo 2024
- febrero 2024
- enero 2024
- diciembre 2023
- noviembre 2023
- octubre 2023
- septiembre 2023
- agosto 2023
- julio 2023
- junio 2023
- mayo 2023
- abril 2023
- marzo 2023
- febrero 2023
- enero 2023
- diciembre 2022
- noviembre 2022
- octubre 2022
- septiembre 2022
- agosto 2022
- julio 2022
- junio 2022
- mayo 2022
- abril 2022
- marzo 2022
- febrero 2022
- enero 2022
- diciembre 2021
- noviembre 2021
- octubre 2021
- septiembre 2021
- agosto 2021
- julio 2021
- junio 2021
- mayo 2021
- abril 2021
- marzo 2021
- febrero 2021
- enero 2021
- diciembre 2020
- noviembre 2020
- octubre 2020
- septiembre 2020
- agosto 2020
- julio 2020
- junio 2020
Calendar
| L | M | X | J | V | S | D |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | ||||
| 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 |
| 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| 25 | 26 | 27 | 28 | 29 | 30 | 31 |
